MOCENSTVÍ PRVKŮ
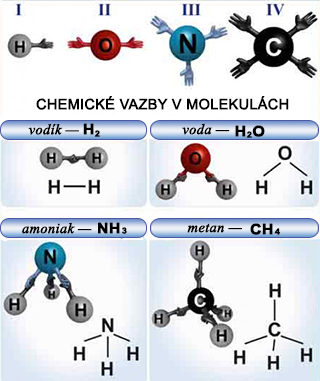
Mocenství, přesněji formální mocenství, je číslo udávající počet atomů vodíku, které může prvek vázat nebo nahradit v jiných sloučeninách. Prvky mohou být jednomocné až osmi-mocné. Na základě takto chápaného mocenství bylo odvozeno chemické názvosloví. Místo formálního mocenství se v současné době používá pojmu oxidační číslo, jehož definice je složitější.
Protože se kyslík slučuje téměř se všemi prvky a tvoří s nimi oxidy, jsou názvy oxidů základem českého chemického názvosloví. Mocenství je vyjádřeno příponou přídavného jména v názvu oxidu. Podle této přípony ihned poznáme mocenství, a tím i počet atomů prvků, které tvoří příslušný oxid
NÁZVOSLOVÍ OXIDŮ
| Mocenství | Poměr počtu atomů | Typ oxidu | Přípona | Příklad oxidu |
| I | 2 : 1 | R2O | -ný | Na2O - oxid sodný |
| II | 1 : 1 | RO | -natý | CaO - oxid vápenatý |
| III | 2 : 3 | R2O3 | -itý | Al2O3 - oxid hlinitý |
| IV | 1 : 2 | RO2 | -ičitý | CO2 - oxid uhličitý |
| V | 2 : 5 | R2O5 | -ečný -ičný |
P2O5 - oxid fosforečný N2O5 - oxid dusičný |
| VI | 1 : 3 | RO3 | -ový | SO3 - oxid sírový |
| VII | 2 : 7 | R2O7 | -istý | Mn2O7 - oxid manganistý |
| VIII | 1 : 4 | RO4 | -ičelý | OsO4 - oxid osmičelý |
CO LZE VYPOČÍTAT Z CHEMICKÝCH VZORCŮ
Chemický vzorec udává hmotnost složení sloučeniny. Ze vzorce a z relativních atomových hmotností prvků (které jsou uvedeny v tabulce prvků) vypočteme i procentové složení. Součet relativních atomových hmotností všech prvků ve sloučenině udává relativní molekulovou hmotnost sloučeniny. A dělíme-li relativní atomovou hmotnost prvku ve sloučenině relativní molekulovou hmotností sloučeniny, dostaneme v procentech množství onoho prvku ve sloučenině.
Příklady: Kolik % vápníku je ve vápenci?
Vápenec (uhličitan vápenatý) CaCO3 má relativní molekulovou hmotnost 100 — je to součet relativních atomových hmotností všech prvků ve vápenci: 40 + 12 + (3 · 16) = 100. Procento vápníku:
40 : 100 = 0,40. Ve vápenci je tedy 40 % vápníku!
Kolik procent olova je v galenitu?
Galenit (sulfid olovnatý) PbS má relativní molekulovou hmotnost 207 + 32 = 239. Obsah olova: 207 : 239 = 0,866. V galenitu je tedy 86,6 % olova.
Kolik krystalické vody je v modré skalici?
Modrá skalice (neboli síran měďnatý) CuSO4·5 H2O má relativní molekulovou hmotnost 63 + 32 + (4 · 16) + 5 · (2 + 16) = 249. Voda má relativní atomovou hmotnost 5 · (2 + 16) = 90. Procento vody je 90 : 249 = 0,361. V modré skalici je tedy 36,1 % vody!